- Todos
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
M
Mapeo génico - Gene mapping
Proceso gracias al cual se determina las posiciones relativas de genes en una molécula de ADN, de un cromosoma o de un plásmido, y de la distancia, dada en unidades de ligamiento o física, que hay entre ellos.
Marcador - Marker
Segmento identificable de ADN (p. ej. RFLP, VNTR, microsatélite) que al presentar una variación amplia entre los individuos, permite analizar su herencia y segregación con los alelos de un gen determinado. Se utiliza en el análisis de ligamiento.
Marcador flanqueante - Flanking marker
Región polimórfica identificable de ADN (es decir, un marcador) localizada en un gen, a diferencia del marcador intragénico, que está localizado dentro de un mismo gen. Los marcadores flanqueantes se utilizan en el análisis de ligamiento para analizar la herencia del gen en cuestión.
Marcador intragénico - Intragenic marker
Región polimórfica identificable de ADN (es decir, un marcador) localizado dentro de la extensión de la secuencia de un gen (es decir, intragénico), a diferencia del marcador flanqueante, que está localizado en uno de los dos lados de un gen. Los marcadores intragénicos se utilizan en el análisis de ligamiento para investigar la herencia del gen en cuestión.
Marco de lectura - Reading frame (sinónimo: exón)
Secuencia de ARN mensajero que es traducido a una cadena de aminoácidos, tres bases al mismo tiempo (triplete) codifican un solo aminoácido.
Marco de lectura abierta - Open reading frame (sinónimo: ORF)
Todos los exones de un gen que contribuyen a los productos proteicos del gen.
Mecanismo de reparación de bases mal emparejadas - Mismatch repair mechanism (sinónimo: reparación de emparejamientos erróneos)
Sistema de control de la integridad del ADN, en el que intervienen determinados genes, que identifica, escinde y corrige los errores de emparejamiento de las bases durante la replicación del ADN. Las mutaciones producidas en los genes responsables de este mecanismo pueden dar lugar a determinadas enfermedades genéticas y algunos tipos de cáncer.
Medicina Personalizada de Precisión - Personalized Precision Medicine
La Medicina Personalizada de Precisión (MPP) se entiende como la identificación y aplicación del abordaje preventivo, diagnóstico y terapéutico más efectivos para cada paciente, utilizando como herramienta la Medicina de Precisión.
Megabase, Mb - Megabase
Unidad de longitud para fragmentos de ADN que equivale a 1 millón de nucleótidos (aproximadamente 1 centimorgan, cM).
Meiosis - Meiosis
Proceso que consiste en dos divisiones celulares consecutivas en los progenitores diploides de las células germinales. Es el proceso por el cual se originan los gametos, que poseen la mitad de cromosomas. Cada una de las dos divisiones de la meiosis tiene las mismas cuatro fases de una mitosis normal: profase, metafase, anafase y telofase.
Metacéntrico - Metacentric
Cromosoma que tiene el centrómero situado aproximadamente en el centro, de modo que los brazos son de longitud similar.
Metafase - Metafase
Fase de la mitosis o la meiosis durante la cual los cromosomas se colocan en el plano ecuatorial de la célula.
Metilación - Methylation
Unión de los grupos metilo a las citosinas del ADN. Se relaciona con una transcripción reducida del gen y se considera el mecanismo principal en la inactivación del cromosoma X y en la impronta genómica.
Metionina - Methionine
La metionina (abreviada como Met o M) es un aminoácido hidrófobo, y esencial. Es uno de los dos aminoácidos codificados por un único codón del código genético, el AUG (el otro es el triptófano, que está codificado por el codón UGG), que es también el mensaje que indica al ribosoma el inicio de la traducción de una proteína desde el ARNm.
Micro RNA (miRNA) - Micro RNA (miRNA)
Los microRNAs (miRNAs) son pequeños RNAs no codificantes. Una de sus funciones conocidas es la regulación postranscripcional de la expresión de genes, mediante la unión a secuencias diana en las regiones 3’UTR (no traducidas) de los ARN mensajeros.
Microarray - Microarray
Superficie sólida sobre la que son depositados y fijados secuencias de genes o fragmentos de genes siguiendo un orden espacial determinado. Se utilizan para estudios de alta densidad, es decir, para analizar muchos genes/miRNAs/SNPs, etc al mismo tiempo en el tejido de interés.
Microdeleción - Microdeletion
Deleción que no puede ser detectada por técnicas citogenéticas clásicas.
Microsatélite - Microsatellite (sinónimos: ADN satélite, repeticiones cortas en tándem)
Segmentos repetitivos de ADN que comprenden de dos a cinco nucleótidos (repeticiones de dinucleótidos/trinucleótidos/ tetranucleótidos/ pentanucleótidos) dispersos por todo el genoma en las regiones no codificadoras que hay entre o dentro de los genes (intrones), se utilizan frecuentemente como marcadores en el análisis de ligamiento debido a la alta variabilidad natural existente en el número de repeticiones entre los individuos. Estas regiones son propiamente inestables y susceptibles a mutaciones.
Mitosis - Mitosis
Proceso por el cual una célula se divide y da lugar a dos células hijas.
Modificación del riesgo - Risk modification
Variación del riesgo genético de un individuo basándose en la información previamente desconocida sobre los antecedentes familiares o en los resultados de los estudios genéticos; dependiendo de la información nueva, el riesgo puede aumentar o disminuir.
Modo de herencia - Mode of inheritance (sinónimos: patrón de herencia)
Manera en la que un determinado rasgo o trastorno genético se transmite de una generación a la siguiente. Ejemplos son el modo de herencia autosómico, dominante y recesivo, el modelo ligado al cromosoma X, dominante y recesivo, y la herencia mitocondrial.
Monosomía - Monosomy
Presencia de sólo uno de la pareja de cromosomas homólogos. La monosomía parcial se refiere a la presencia de una sola copia de un segmento de un cromosoma.
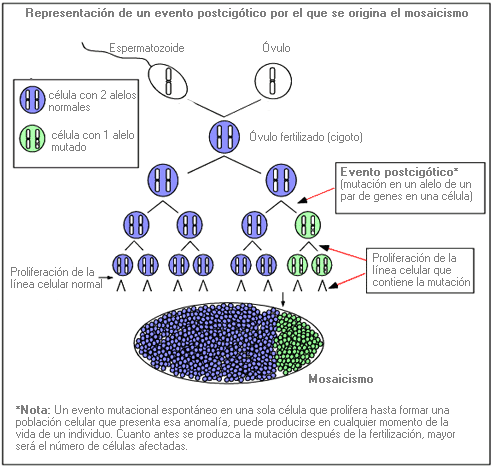
Mosaicismo - Mosaicism
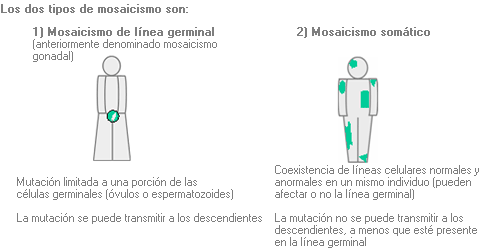
Mosaicismo de línea germinal - Germline mosaicism
Presencia simultánea de dos o más líneas celulares genética o citogenética confinadas a la línea germinal (óvulos o espermatozoides); anteriormente se denominaba mosaicismo gonadal.
Mosaicismo gonadal - Gonadal mosaicism
Véase Mosaicismo de línea germinal.
Mosaicismo somático - Somatic mosaicism
Dos o más líneas celulares que varían en su constitución genética o citogenética en las células del organismo (puede incluir o no las células germinales).
Mutación - Mutation (sinónimos: alteración de la secuencia, mutación del splicing)
Cualquier alteración producida en un gen con respecto a su estado natural; puede ser patológica o una variante no patológica.
1. Mutaciones patológicas: aquellas que dan lugar a una función anormal del gen y a un fenotipo de enfermedad. Los tipos de mutaciones patológicas son los siguientes:


Adaptado de Thompson & Thompson Genetics in Medicine, 6th Edition; RL Nussbaum, RR McInnes, HF Willard, Genetic Variation in Individuals: Mutation and Polymorphism,pág 81, Copyright 2001, con permiso de Elsevier
2. Polimorfismos (variantes normales): Mutaciones que no tienen efectos adversos sobre la función del gen y no dan lugar a un fenotipo alterado (enfermedad).
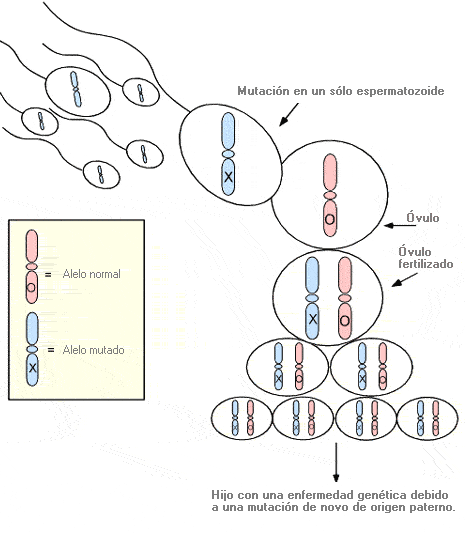
Mutación de línea germinal - Germline mutation
Presencia de un gen alterado en el óvulo o espermatozoide (célula germinal) que puede transmitirse a las generaciones siguientes.
En un individuo, la mutación puede darse en una de cuatro situaciones posibles:
1.- Exclusivamente en una sola célula germinal (óvulo o espermatozoide).
2.- Exclusivamente en las células somáticas (células del organismo, pero NO en la línea germinal); son las normalmente asociadas al desarollo de un tumor.
3.- En algunas células germinales y en otras somáticas.
4.- En todas las células del organismo.


Mutación de novo - De novo mutation (sinónimos: mutación génica de novo, mutación génica nueva, mutación nueva)
Mutación de sentido erróneo - Missense mutation
Sustitución de un solo par de bases que da lugar a la traducción de un aminoácido diferente en esa posición.
Mutación dominante negativa - Dominant negative mutation
Mutación cuyo producto génico afecta de forma adversa al producto génico normal de tipo salvaje de la misma célula, normalmente al dimerizarse (combinarse) con él. En las moléculas poliméricas, tales como el colágeno, las mutaciones dominantes negativas suelen ser más deletéreas que las que no originan ningún producto génico (mutaciones nulas o alelos nulos).
Mutación en el sitio de corte y empalme (splicing) - Splicing
Mutación que altera o suprime la secuencia específica que indica el sitio en el que tiene lugar el splicing de un intrón. A consecuencia de estas mutaciones, uno o más intrones permanecen en el ARN mensajero maduro y pueden alterar la generación del producto proteico.
Mutación familiar específica - Familial mutation
En una familia, la alteración observada en una secuencia que causa una determinada enfermedad o predispone a ella; la mutación puede ser rara o común.
Mutación intrónica - Intronic mutation
Mutación (normalmente una sustitución de bases) localizada en un intrón que genera un sitio de corte y empalme (splicing) alternativo que compite con los sitios de splicing normales durante el procesamiento del ARN. Esta mutación da lugar a la formación de ARN mensajero maduro con secuencias intrónicas.
Mutación no descrita - Novel mutation
Alteración nueva de un gen, que no ha sido previamente descrita. No debe confundirse con mutación “nueva” o “de novo”.
Mutación particular - Private mutation (sinónimo: mutación única)
Tipo de mutación patológica rara que se observa sólo en unas pocas familias.
Mutación patológica - Disease
Alteración en un gen que causa o predispone a un individuo a desarrollar una enfermedad específica.
Mutación por cambio de marco - Frameshift mutation (sinónimos: deleción fuera de marco, mutación fuera de marco)
Inserción o deleción de una secuencia de pares de bases que no es múltiplo de tres y por lo tanto, altera el marco de lectura del triplete, lo que da lugar normalmente a la creación de un codón de terminación (parada) prematuro y cuyo resultado es un producto proteico truncado.
Mutación predisponente - Predisposing mutation (sinónimo: gen de susceptibilidad)
Mutación génica que incrementa la susceptibilidad o predisposición de un individuo a desarrollar una determinada enfermedad. Cuando se heredan mutaciones patogénicas en estos genes de susceptibilidad, es probable, pero no seguro, que el individuo desarrolle síntomas de la enfermedad.
Mutación puntual - Point mutation
Alteración en la secuencia del ADN causada por el cambio, inserción o deleción de un único nucleótido.
Mutación sin cambio de pauta de lectura - In-frame mutation
Mutación que no produce un cambio en el marco de lectura del triplete cuando se produce la transcripción de ADN a ARN mensajero. Estas mutaciones, sin embargo, pueden dar lugar a la síntesis de un producto proteico anormal si, al traducirse el ARN a proteína, el cambio de triplete supone un cambio de aminoácido.
Mutación sin sentido - Nonsense mutation
Mutación que altera un codón convirtiéndolo en uno de terminación (stop codon) prematura del proceso de traducción.
Mutagénico - Mutagenic
Capaz de inducir cambios en la información genética de una célula.