- Todos
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
E
Estudios de repeticiones de trinucleótidos - Trinucleotide repeat testing
Análisis genético cuyo objetivo es la cuantificación del número de repeticiones de grupos de tres nucleótidos en un segmento determinado de ADN.
Para cuantificar las repeticiones de trinucleótidos, se pueden utilizar dos tipos de análisis mutacional que se representan en el diagrama siguiente:
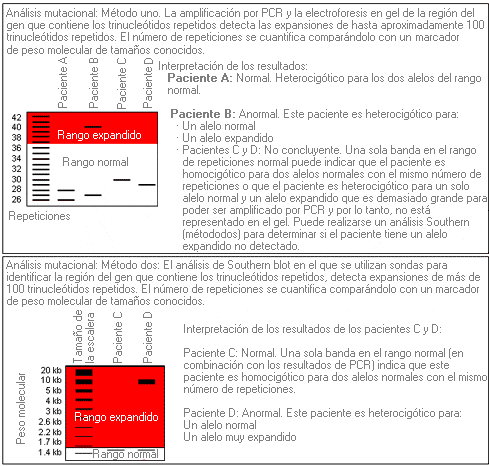
Algunas implicaciones clínicas:
El análisis Southern blot no se realiza de forma rutinaria en todos los laboratorios para clarificar la interpretación de los resultados de las bandas no concluyentes por PCR. Cuando se reciba un informe de un número de repeticiones “homocigóticas” normales, particularmente en un niño sintomático de corta edad que podría presentar una expansión grande, es recomendable que el médico confirme que se ha realizado el análisis Southern blot para evaluar la posibilidad de que haya una repetición de trinucleótidos muy expandida.
Si no está disponible el análisis Southern blot, se puede realizar un análisis mutacional basado en PCR/electroforesis en gel de los padres de un paciente con un número de repeticiones “homocigóticas” normales, para determinar si el paciente podría haber heredado de sus padres dos alelos con el mismo número de repeticiones.
N
Nucleótido - Nucleotide
Molécula compuesta por una base nitrogenada (adenina, guanina, timina o citosina en ADN; adenina, guanina, uracilo o citosina en ARN), un grupo fosfato y un azúcar (desoxirribosa en ADN; ribosa en ARN). El ADN y el ARN son polímeros de muchos nucleótidos.
O
Oligonucleótidos específicos del alelo - Allele-specific oligonucleotide testing (ASO)
Prueba de genética molecular empleada para la detección de una mutación específica por medio de un segmento sintético de ADN de una longitud aproximada de 20 pares de bases (oligonucleótido). El investigador diseña la secuencia específica que se une a la secuencia complementaria en una muestra de ADN problema, lo que permite su identificación.
P
Polimorfismo de nucleótido único - Single Nucleotide Polymorphism o SNP
Variación en la secuencia de ADN que implica una sola base: adenina (A), timina (T), citosina (C) o guanina (G). Son los polimorfismos genéticos más frecuentes y se considera que determinan gran parte de la variabilidad genética entre individuos. Se conocen varios millones de SNP repartidos por todos los cromosomas humanos, aproximadamente 1 cada 300-100 pares de bases. La frecuencia de un SNP en población general se sitúa por encima del 1%.
Diversas técnicas de análisis masivo del genoma se fundamentan en el estudio de miles o millones de SNP que cubren la práctica totalidad del genoma (Genome Wide Association Studies, o GWAS), para buscar la asociación de algunos de ellos con enfermedades concretas, utilizando para ello grandes números tanto de individuos enfermos, como de individuos sanos.
R
Repetición de trinucleótidos - Trinucleotide repeat
Secuencias de tres nucleótidos que se repiten varias veces en tándem en un mismo gen. La variación polimórfica normal en el número de repeticiones, que carece de significación clínica, ocurre normalmente entre los individuos. Los alelos anormalmente grandes se clasifican de menor a mayor tamaño en alelos mutables normales, alelos de penetrancia reducida y alelos de penetrancia completa, respectivamente.
La secuencia de un alelo que contiene cuatro repeticiones CAG tiene la estructura siguiente:
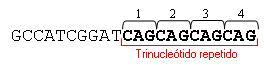
Un trinucleótido repetido con nueve repeticiones CCG tiene la estructura siguiente:
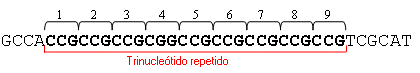
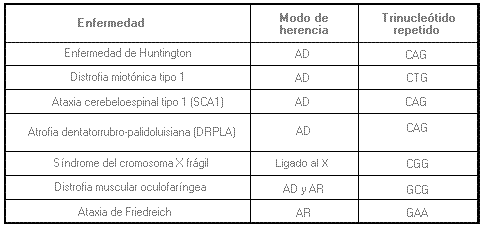
1. A diferencia de otros alelos que son estables de una generación a otra, los alelos que contienen repeticiones de trinucleótidos son inestables y dinámicos y pueden experimentar una expansión cuando son transmitidos de una generación a la siguiente. Las expansiones grandes del número de repeticiones pueden causar anomalías en la función y expresión de un gen. A continuación, se proporcionan algunos ejemplos de trastornos genéticos causados por expansiones de trinucleótidos repetidos:
2. Las expansiones causantes de enfermedad, pueden ser pequeñas (A) o grandes (B).
A) Distrofia muscular oculofaríngea
Tamaño de los alelos normales: 6 repeticiones GCG
Tamaño de los alelos de penetrancia completa: 8-13 repeticiones GCG.
B) Distrofia miotónica1
Tamaño de los alelos normales: <30 repeticiones CTG
Tamaño de los alelos de penetrancia completa: 80-2000 repeticiones CTG
3. En algunos trastornos causados por repetición de trinucleótidos, tales como el síndrome del cromosoma X frágil, existe un rango de repeticiones de alelos mutables normales que son inestables y tienden a expandirse cuando son transmitidos de una generación a la siguiente. Los individuos con alelos mutables normales no suelen resultar afectados.
Síndrome del cromosoma X frágil
Tamaño de los alelos normales: ≤58 repeticiones CGG
Tamaño de los alelos mutables normales: 59- ~ 200 repeticiones CGG
Tamaño de los alelos de penetrancia completa: <200 repeticiones CGG
En algunos trastornos causados por repetición de trinucleótidos, tales como la enfermedad de Huntington, existe un rango de alelos de penetrancia reducida (36-39 alelos), por lo que uno de estos alelos podría dar lugar a una enfermedad de comienzo muy tardío y a ninguna manifestación clínica de la enfermedad durante la vida del individuo.
Enfermedad de Huntington
Tamaño de los alelos normales: ≤26 repeticiones CAG
Tamaño de los alelos mutables normales: 27-35 repeticiones CAG
Tamaño de los alelos de penetrancia reducida: 36-39 repeticiones CAG
Tamaño de los alelos de penetrancia completa: ≥40 repeticiones CAG