- Todos
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
A
ADN (Ácido desoxirribonucleico) - DNA ( Deoxyribonucleic acid)
Es la molécula portadora la información genética, que posibilita su transmisión de una generación a la siguiente.
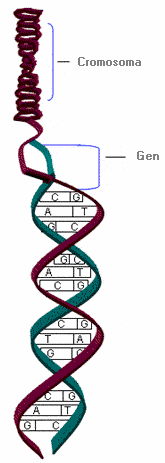
El ADN está constituido por dos cadenas de nucleótidos complementarias unidas entre sí por puentes de hidrógeno, enrollada la una sobre la otra formando una doble hélice. El elemento esencial del ADN es el nucleótido formado por un azúcar, la desoxirribosa, una base nitrogenada y un grupo fosfato. Las bases nitrogenadas son purinas: Adenina (A) y Guanina (G), y pirimidinas: Timina (T) y Citosina (C). Estas bases se unen al carbono 1 de la desoxirribosa para formar los nucleósidos, que a la vez se unirán con los grupos fosfato para formar los nucleótidos. Las bases nitrogenadas se unen de manera específica, guanina con citosina y adenina con timina, mediante puentes de hidrógeno.
El orden o secuencia de nucleótidos es la estructura primaria del ADN. La información genética reside en la secuencia de bases. Los genes son segmentos del ADN que codifican para proteínas. El orden de las bases en el gen determina la secuencia de aminoácidos que compondrán la proteína.
En las células eucariotas, el ADN se encuentra en el núcleo celular formando los cromosomas.
ADNc - cADN
ADN complementario, generado a partir del molde de ARN, mediante la retrotranscripción del ARNm maduro.
Análisis basados en ADN - DNA-based analysis
Pruebas que implican el estudio de ADN mediante un análisis de ligamiento, secuenciación o cualquiera de los diferentes métodos utilizados para la detección de mutaciones.
Análisis de ligamiento - Linkage analysis (sinónimo: análisis indirecto del ADN)
Estudio de los polimorfismos de las secuencias de ADN (variantes normales) que están próximos a/o dentro de un gen de interés (ligamiento) para identificar, en una misma familia, la segregación de una mutación patológica en un gen determinado.
EXPLICACIÓN:
Las tres fases del análisis de ligamiento son las siguientes:
1. Establecer los haplotipos de cada individuo: Se analizan los múltiples marcadores de ADN dispuestos a cada lado (marcadores flanqueantes) o dentro (marcadores intragénicos) de la región del gen de interés, con objeto de determinar el conjunto de marcadores (haplotipos) de cada miembro de la familia.
2. Establecer la fase, comparando los haplotipos entre los miembros de la familia: Mediante la comparación de los haplotipos de los miembros de la familia con un estado genético conocido (es decir, afectados, no afectados), se puede identificar el haplotipo asociado con el alelo patológico.
3. Determinar el estado genético: Una vez establecido el haplotipo asociado con la enfermedad, es posible determinar el estado genético de los miembros de una familia de riesgo.
Ejemplo: Análisis de ligamiento para el diagnóstico prenatal de una enfermedad ligada al cromosoma X.
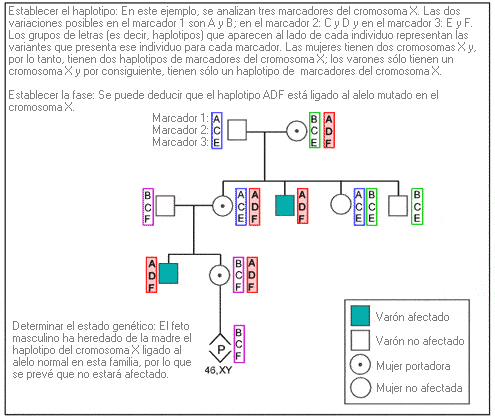
Algunas implicaciones clínicas
El análisis de ligamiento se utiliza generalmente cuando el análisis de ADN directo no es viable, porque se desconoce el gen de interés o no se puede detectar una mutación en ese gen en una familia específica.
En la mayoría de los casos, el haplotipo en sí carece de significación; sólo tiene sentido en el contexto de un estudio familiar. Sólo en el caso raro de que el desequilibrio del ligamiento sea un haplotipo específico, habrá una probabilidad muy elevada de que esté asociado con una mutación patológica específica.
La exactitud del análisis de ligamiento depende de:
La exactitud del diagnóstico clínico en un miembro o miembros de la familia que estén afectados.
La distancia entre la mutación patológica y los marcadores. El análisis de ligamiento puede proporcionar resultados falso positivo o falso negativo si, durante la formación de los gametos (meiosis), se produce recombinación que implique a los marcadores y suponga un intercambio entre el material genético de los cromosomas heredados de la madre o del padre. El riesgo de recombinación es proporcional a la distancia entre la mutación patológica y los marcadores. El riesgo de recombinación es más bajo si se utilizan marcadores intragénicos.
La informatividad de los marcadores genéticos en la familia del paciente. Si la secuencia de ADN de una variante determinada difiere entre los cromosomas heredados de la madre y del padre, este marcador es informativo. Por el contrario, si la secuencia de ADN de una variante determinada no difiere entre los dos cromosomas, el marcador no es informativo.
Análisis de matrices de ADN - DNA microarray analysis
Análisis directo del ADN - Direct DNA analysis
La utilización de técnicas de secuenciación, análisis mutacional, rastreo de mutaciones o cualquier otro medio de estudio molecular genético, para detectar variantes en un gen que pueden estar asociadas a trastornos genéticos específicos. El análisis directo del adn es posible sólo cuando se conoce el gen o genes o la región genómica, asociados con la enfermedad.
Las técnicas utilizadas para el análisis de ADN directo pueden ser las siguientes:
Análisis de secuencias
Rastreo de mutaciones (p. ej. CSGE, DHPLC, SSCP)
Análisis mutacional (p. ej. PCR, Southern blot, análisis de repeticiones de trinucleótidos, FISH, análisis de truncación de proteínas (PTT), estudios de heterocigosidad, análisis RFLP, ASO)
El análisis de ADN directo contrasta con el análisis de ligamiento (que anteriormente se denominaba análisis de ADN indirecto)
Algunas implicaciones clínicas
El análisis de ADN directo sólo es posible cuando se conoce el gen (genes) o la región genómica asociados con una enfermedad
El análisis de ligamiento se puede realizar cuando no se conoce el gen o los genes asociados con una enfermedad
B
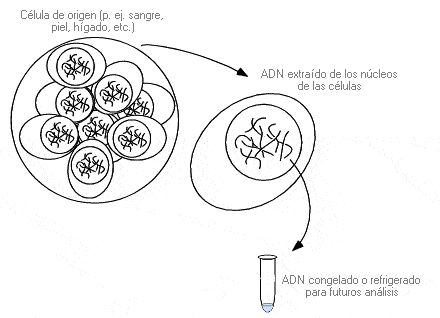
Banco de ADN - DNA banking
Proceso de almacenaje durante un periodo indefinido del adn extraído de cualquiera de las posibles fuentes celulares, conservado bajo congelación o refrigeración para futuros análisis.
C
cADN, Librería de - cDNA library
Colección de secuencias de adn generadas a partir de la secuencia del ARN mensajero (mARN). Estas librerías contienen sólo adn codificante de proteínas (genes), quedando excluídas las secuencias de adn que no codifican.
E
Estudios de genética molecular - Molecular genetic testing (sinónimos: análisis de ADN, análisis basados en ADN, estudios moleculares)
Pruebas que implican el estudio del ADN, mediante análisis de ligamiento, secuenciación o detección de mutaciones, utilizando uno o varios de los diferentes métodos disponibles.
M
Microsatélite - Microsatellite (sinónimos: ADN satélite, repeticiones cortas en tándem)
Segmentos repetitivos de ADN que comprenden de dos a cinco nucleótidos (repeticiones de dinucleótidos/trinucleótidos/ tetranucleótidos/ pentanucleótidos) dispersos por todo el genoma en las regiones no codificadoras que hay entre o dentro de los genes (intrones), se utilizan frecuentemente como marcadores en el análisis de ligamiento debido a la alta variabilidad natural existente en el número de repeticiones entre los individuos. Estas regiones son propiamente inestables y susceptibles a mutaciones.
R
Replicación del ADN - DNA replication
La replicación del ADN es el proceso mediante el cual se duplica una molécula (sintetiza una copia idéntica) de ADN. Cuando una célula se divide, en primer lugar, debe duplicar su genoma para que cada célula hija contenga un juego completo de cromosomas. De esta manera se garantiza la transmisión de la información genética.
S
Secuenciación del ADN - DNA sequencing
Es el conjunto de métodos que tienen por objetivo determinar el orden exacto de los nucleótidos (A, C, G y T) en la molécula de ADN. La secuencia de bases de ADN lleva la información que una célula necesita para originar moléculas de ARN y proteínas. Los avances en las técnicas de secuenciación de ADN han sido muy notables en los años recientes gracias al Proyecto Genoma Humano. Es posible aplicar estas técnicas para conocer la secuencia de un único gen, de varios genes (paneles), al conjunto de genes de un individuo (exoma) o, finalmente a todo el genoma de un individuo.
El método de secuenciación del ADN desarrollado por Frederick Sanger y colaboradores en 1977 ha sido el de uso más extendido en los últimos 40 años. En los años más recientes ese método está siendo sustituido por la secuenciación de nueva generación (“next-generation sequencing”, NGS, o los términos sinónimos “massively parallel” o “deep sequencing”) que ha revolucionado el mundo de la investigación biomédica al ser capaz de analizar simultáneamente millones de pequeños fragmentos de ADN. La tecnología de NGS permite disponer en horas de la secuencia del exoma o del genoma humano completo.