- Todos
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
D
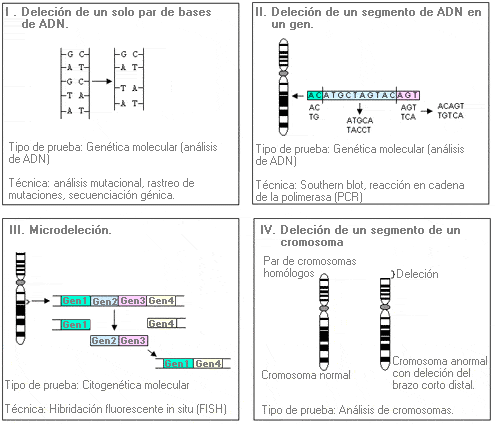
Deleción - Deletion
Alteración genética consistente en la pérdida de un segmento de ADN. Su magnitud es variable, pudiendo ser tan pequeñas como un solo par de bases o tan grandes que afecten a uno o más genes.
M
Microdeleción - Microdeletion
Deleción que no puede ser detectada por técnicas citogenéticas clásicas.
S
Síndrome de microdeleción - Microdeletion syndrome (sinónimo: síndrome de deleción de genes contiguos)
Síndrome causado por una deleción cromosómica que comprende varios genes y es demasiado pequeña para poder ser detectada al microscopio utilizando métodos citogenéticos convencionales. Dependiendo del tamaño de la deleción, se pueden utilizar ocasionalmente otras técnicas, tales como FISH u otros métodos de análisis de ADN, para su identificación.